A estrutura do núcleo de uma célula tem sido uma pista visível sobre se uma célula está saudável ou doente. Embora os cientistas tenham feito grandes progressos na compreensão dos genes e das suas funções, tem sido muito difícil ligar diretamente o que vemos ao microscópio com o que está a acontecer no nosso ADN. Agora, um novo método ajuda a unir esses dois mundos.
Zachary Chiang e Carolyn Comenho da Universidade de Harvard e Dr. Os pesquisadores, liderados por Jason Buenrostro, desenvolveram uma nova técnica chamada Sequenciamento do Genoma In Situ de Expansão (XIGS). O estudo é publicado na revista Science.
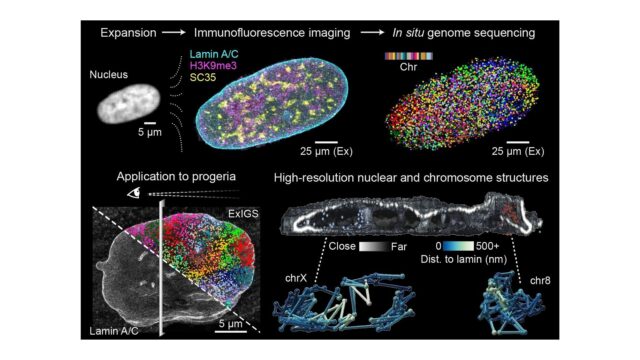
O ExIGS dá aos pesquisadores a capacidade de observar o DNA e as proteínas críticas dentro do núcleo – o centro de controle de uma célula – em grande detalhe. Ao contrário das técnicas anteriores, permite aos cientistas ver como estas moléculas estão organizadas no espaço e como interagem. A equipe usou o método para estudar células de uma pessoa com síndrome de progéria de Hutchinson-Gilford (HGPS), uma doença rara que faz com que as crianças envelheçam rapidamente.
Eles encontraram uma conexão inesperada entre as formas anormais desses núcleos celulares e o silenciamento de certos genes. Nas células saudáveis, a eucromatina, a forma ativa e fraca de DNA sobre a qual os genes são direcionados, mantém a célula funcionando normalmente. Mas nas células da Progéria, descobriu-se que esse DNA normalmente ativo estava envolvido em certas regiões. Isto sugere que mudanças na forma fetal podem ser suficientes para desligar genes importantes.
“Anormalidades na lamina estão ligadas a pontos críticos de repressão aberrante da eucromatina que podem destruir a identidade celular”, disse o Dr. Buenostro. As proteínas laminas fazem parte da subcamada do embrião. Isto significa que, se este sistema de suporte falhar, poderá silenciar os genes que conferem às células os seus papéis únicos.
Para confirmar a fiabilidade do seu método, os investigadores mostraram que o ExIGS preserva a estrutura natural do embrião, ao mesmo tempo que fornece detalhes extremamente nítidos – até dez vezes mais do que os métodos de sequenciação anteriores. Eles combinaram isso com marcação fluorescente, uma forma de fazer moléculas específicas acenderem para que possam ser rastreadas para ver como os cromossomos – as estruturas que contêm o DNA – se movem e como essas mudanças estão ligadas à atividade genética.
“A presença de anormalidades de Lamin está associada a um aumento na frequência de ambientes desordenados”, disse o Dr. Labade. Embora estas anomalias estejam claramente ligadas a alterações na função genética, elas não atraem diretamente a eucromatina para elas, observou ele. Em vez disso, o efeito é mais pegajoso e local, em vez de afetar todo o núcleo uniformemente.
As suas observações revelaram que mesmo dentro de uma única célula, as regiões afetadas por estas mudanças estruturais são imprevisíveis. Esses pontos problemáticos podem se espalhar e afetar partes do genoma, um bloco inteiro de material genético envolvido na comunicação entre células. Essa inconsistência pode dificultar o ajuste dos resultados.
Xiang relembrou os anos de esforço necessários para chegar a este ponto: “O projeto nada mais era do que uma ideia maluca: ser capaz de sequenciar genes diretamente dentro do núcleo. Ele também refletiu sobre a importância do financiamento contínuo para este tipo de ciência de alto risco e alta recompensa. Embora o projecto tenha obtido uma boa pontuação num concurso nacional de financiamento de investigação, esse apoio foi subitamente retirado devido a questões políticas mais amplas que afectavam os orçamentos científicos.
A importância desta nova ferramenta vai além de apenas uma doença. ExIGS abre a porta para investigar como as mudanças na forma e estrutura fetal podem desempenhar um papel no envelhecimento, no câncer e em muitas outras condições. Ele fornece uma maneira de finalmente conectar o que vemos no microscópio ao modo como nossos genes funcionam.
Nota de diário
Labade AS, Chiang ZD, Comenho C., Reginato PL, Payne AC, Earl AS, Shrestha R., Duarte FM, Habibi E., Zhang R., Church GM, Boyden ES, Chen F., Buenrostro JD Repressão de eucromatina.” bioRxiv, 2024. DOI: https://doi.org/10.1101/2024.09.24.614614
Sobre os professores
Dr.Jason Buenostro Ele é um pesquisador líder na área de regulação genética e genômica de célula única. Baseado na Universidade de Harvard e no Broad Institute, ele foi pioneiro em diversas técnicas que revelam como as células organizam e regulam seu DNA, incluindo o método ATAC-seq amplamente adotado. O seu trabalho centra-se no desenvolvimento de tecnologias que ligam a organização espacial de um gene ao seu estado funcional, com o objetivo de compreender como estes processos funcionam mal em doenças como o cancro e o envelhecimento. Para treinar a próxima geração de cientistas e promover ambientes de pesquisa abertos e inovadores, o Dr. Sua abordagem interdisciplinar combina biologia molecular, bioengenharia e ciência computacional.

Dr. Um geneticista conhecido por suas contribuições à análise genética espacial e ao mapeamento de DNA de alta resolução em células individuais. Como cientista da Universidade de Harvard e do Broad Institute, ele foi fundamental no desenvolvimento do sequenciamento do genoma in situ de expansão (XIGS), um método que visualiza DNA e proteínas nucleares com precisão em nanoescala. Os seus interesses de investigação situam-se na intersecção do desenvolvimento tecnológico e da descoberta biológica, particularmente como as mudanças físicas na célula podem afectar a função genética. Dr. Chiang é um defensor de um financiamento acadêmico robusto e de práticas de pesquisa transparentes. Anunciou recentemente a sua reforma do meio académico, reflectindo os desafios de sustentar projectos ambiciosos e de longo prazo num cenário científico em mudança.

Dr. Ele é biólogo molecular e inovador tecnológico especializado em sequenciamento de genoma e análise espacial de células. Na Universidade de Harvard e no Broad Institute, ele co-desenvolveu o ExIGS, que permite aos cientistas estudar a organização física e funcional dos genes dentro de células intactas. Com forte foco na ciência básica e no rigor experimental, o Dr. Labade passou anos refinando ferramentas que conectam estruturas celulares microscópicas a padrões genéticos em grande escala. Sua abordagem combina testes de laboratório úmido com imagens avançadas e modelagem computacional. Acreditando firmemente no poder da ciência movida pela paixão, o Dr. Labade enfatizou a importância da liberdade acadêmica e do investimento de longo prazo em pesquisas de alto risco e alta recompensa.
Caroline Comenho Um cientista emergente na área de genômica celular, fazendo contribuições significativas para o desenvolvimento de técnicas de sequenciamento de genoma de alta resolução. No Broad Institute e na Universidade de Harvard, colaborou na plataforma ExIGS, que permite o mapeamento espacial preciso do DNA dentro do núcleo celular. Seu trabalho se concentra na compreensão de como a estrutura fetal afeta a expressão genética, particularmente no envelhecimento e em condições relacionadas a doenças. Comenho combina experiência em biologia molecular com uma base sólida em tecnologias de imagem para ajudar a preencher a lacuna entre os dados de sequenciamento e as características visuais das células. Ele representa uma nova onda de pesquisadores impulsionados tanto pela inovação tecnológica quanto pela inteligência biológica.